没有合适的资源?快使用搜索试试~ 我知道了~
高中化学选修4知识点分类总结.doc
1.该资源内容由用户上传,如若侵权请联系客服进行举报
2.虚拟产品一经售出概不退款(资源遇到问题,请及时私信上传者)
2.虚拟产品一经售出概不退款(资源遇到问题,请及时私信上传者)
版权申诉
0 下载量 83 浏览量
2021-10-11
16:15:09
上传
评论
收藏 145KB DOC 举报
温馨提示

试读
17页
高中化学选修4知识点分类总结.doc
资源推荐
资源详情
资源评论
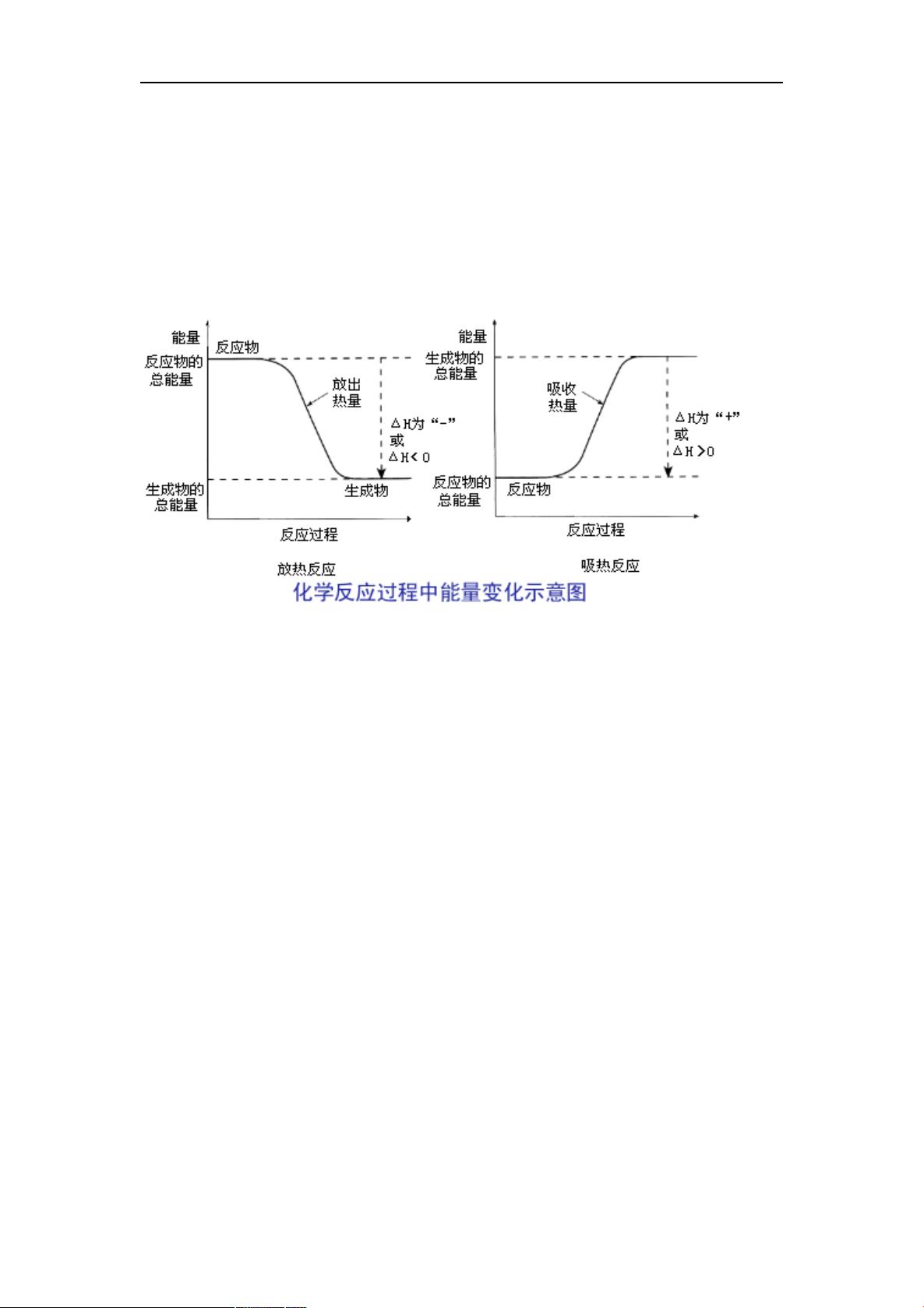
第一章 化学反响与能量
一、焓变反响热
.反响热:化学反响过程中所放出或吸收的热量,任何化学反响都有反响热 ,
因为任何化学反响都会存在热量变化,即要么吸热要么放热。反响热可以分为
〔燃烧热、中和热、溶解热〕
.焓变的意义:在恒压条件下进展的化学反响的热效应
符号: △单位:,即:恒压下:焓变反响热,都可用 表
示,单位都是 。
产生原因:化学键断裂——吸热化学键形成——放热
放出热量的化学反响。放热吸热为“〞或△
吸收热量的化学反响。〔吸热放热〕△为“〞或△
也可以利用计算△ 来判断是吸热还是放热。△生成物所具有的总能量反
响物所具有的总能量反响物的总键能生成物的总键能
常见的放热反响:① 所有的燃烧反响② 所有的酸碱中和反响③ 大多数的
化合反响④ 金属与水或酸的反响⑤ 生石灰〔氧化钙〕和水反响⑥铝热反响等
常见的吸热反响:① 晶体
与
大多数的分解反响
③ 条件一般是加热或高温的反响
区分是现象〔物理变化〕还是反响〔生成新物质是化学变化〕,一般 铵盐
溶解是吸热现象,别的物质溶于水是放热。
能量与键能的关系:物质具有的能量越低,物质越稳定,能量和键能成反比。
!同种物质不同状态时所具有的能量:气态液态固态
"常温是指 !,标况是指 #
$比拟△ 时必须连同符号一起比拟。
二、热化学方程式
定义:表示参加反响物质的量和反响热的关系的化学方程式。
书写化学方程式注意要点 %& 热化学方程式必须标出能量变化,即反响热
△,△ 对应的正负号都不能省。
热化学方程式中必须标明反响物和生成物的聚集状态〔'##( 分别表示固态,
液态,气态,水溶液中溶质用 ) 表示〕
* 热化学反响方程式不标条件,除非题中特别指出反响时的温度和压强。
+ 热化学方程式中的化学计量数表示物质的量,不表示个数和体积,可以是整
1 / 17

数,也可以是分数
, 各物质系数加倍,△ 加倍,即:△ 和计量数成比例;反响逆向进展,
△ 改变符号,数值不变。
"表示意义:物质的量—物质—状态—吸收或放出-热量。
三、燃烧热
.概念: . 时, 纯物质完全燃烧生成稳定的氧化物〔二氧化碳、
二氧化硫、液态水
〕时所放出的热量。燃烧热的单位用 表示。
/注意以下几点:
& 研究条件:.
反响程度:完全燃烧,产物是稳定的氧化物。
* 燃烧物的物质的量:
+ 研究容:放出的热量。〔,单位 〕
燃烧热和中和热的表示方法都是有 时才有负号。
石墨和金刚石的燃烧热不同。不同的物质燃烧热不同。
四、中和热
.概念:在稀溶液中,酸跟碱发生中和反响而生成
,这时的反响
热叫中和热。
.强酸与强碱的中和反响其实质是 和 反响,其热化学方程式为:
))
-!$
.弱酸或弱碱电离要吸收热量,所以它们参加中和反响时的中和热小于
!$。
.中和热的测定实验:看课本装置图
〔〕一般用强酸和强碱做实验,且碱要过量〔如果酸和碱的物质的量一样,
中和热会偏小〕,一般中和热为 !$。
〔〕假设用弱酸或弱碱做实验,放出的热量会偏小,中和热会偏小。
〔〕假设用浓溶液做实验,放出的热量会偏大,中和热会偏大。
在试验中,增大酸和碱的用量,放出的热量会增多但中和热保持不变。
五、盖斯定律
.容:化学反响的反响热只与反响的始态〔各反响物〕和终态〔各生成物〕
有关,而与具体反响进展的途径无关,如果一个反响可以分几步进展,那么各
分步反响的反响热之和与该反响一步完成的反响热是一样的。
方法: 写出目标方程式0
确定“中间产物〞〔要消去的物质〕0
变换方程式# 要同时变化
然后用消元法逐一消去“中间产物〞0
得到目标方程式并进展相应的运算。
六、能源
注:水煤气是二次能源。
2 / 17

第二章 电化学根底
第一节 原电池
原电池:
、概念:化学能转化为电能的装置叫做原电池
、组成条件:①两个活泼性不同的电极② 电解质溶液③ 电极用导线相连并
插入电解液构成闭合回路
、电子流向:外电路:负极——导线——正极
电路:盐桥中 阴离子移向负极的电解质溶液,盐桥中 阳 离子移向正
极的电解质溶液。
、电极反响:以锌铜原电池为例:
负极:氧化反响:Zn-2e=Zn
2
+
较活泼金属〕
正极:复原反响:2H
+
+2e=H
2
↑〔较不活泼金属〕
总反响式:Zn+2H
+
=Zn
2+
+H
2
↑
!、正、负极的判断:
〔〕从电极材料:一般较活泼金属为负极;或金属为负极,非金属为正极。
〔〕从电子的流动方向 负极流入正极
〔〕从电流方向 正极流入负极
〔〕根据电解质溶液离子的移动方向 阳离子流向正极,阴离子流向负极
〔!〕根据实验现象①11溶解的一极为负极11 增重或有气泡一极为正极
第二节 化学电池
、电池的分类:化学电池、太阳能电池、原子能电池
、化学电池:借助于化学能直接转变为电能的装置
、化学电池的分类: 一次电池 、 二次电池 、 燃料电池
一、一次电池
、常见一次电池:碱性锌锰电池、锌银电池、锂电池等
二、二次电池
、二次电池:放电后可以再充电使活性物质获得再生,可以屡次重复使用,
又叫充电电池或蓄电池。
、电极反响:铅蓄电池
放电:负极〔铅〕:.2+ -e
3
=.24
5
正极〔氧化铅〕:.2
+
+ +e
3
=.24
5+
充电:阴极:.24
+
-e
3
=.2
+
+
阳极:.24
+e
3
=.2+
两式可以写成一个可逆反响:.2
+.2+
4
.24
5+
、目前已开发出新型蓄电池:银锌电池、镉镍电池、氢镍电池、锂离子电池、
聚合物锂离子电池
三、燃料电池
、燃料电池:是使燃料与氧化剂反响直接产生电流的一种原电池
、电极反响:一般燃料电池发生的电化学反响的最终产物与燃烧产物一样,
可根据燃烧反响写出总的电池反响,但不注明反响的条件。,负极发生氧化反
3 / 17
放电
充电
响,正极发生复原反响,不过要注意一般电解质溶液要参与电极反响。 以氢氧
燃料电池为例,铂为正、负极,介质分为酸性、碱性和中性。
当电解质溶液呈酸性时:
负极:
-6
3
正极:O
+ e
3
当电解质溶液呈碱性时:
负极:
+
3
-6
3
=
正极:O
+
+ e
3
=
3
另一种燃料电池是用金属铂片插入 7 溶液作电极,又在两极上分别通甲烷
燃料和氧气氧化剂。电极反响式为:
负极:+--63=+$;
正极:++6=3。
电池总反响式为:++7=7+
、燃料电池的优点:能量转换率高、废弃物少、运行噪音低
四、废弃电池的处理:回收利用
第三节 电解池
一、电解原理
、电解池:把电能转化为化学能的装置也叫电解槽
、电解:电流外加直流电通过电解质溶液而在阴阳两极引起氧化复原反响
被动的不是自发的的过程
、放电:当离子到达电极时,失去或获得电子,发生氧化复原反响的过程
、电子流向:
〔电源〕负极—〔电解池〕阴极—〔离子定向运动〕电解质溶液—〔电解池〕
阳极—〔电源〕正极
!、电极名称与反响:
阳极:与直流电源的 正极 相连的电极,发生 氧化 反响
阴极:与直流电源的 负极 相连的电极,发生 复原 反响
"、电解 8
溶液的电极反响:
阳极:
6
氧化
阴极:8
68复原
总反响式:8
8
↑
$、电解本质:电解质溶液的导电过程,就是电解质溶液的电解过程
规律总结:电解反响离子方程式书写:
放电顺序:
阳离子放电顺序
9(
(
:6
8
〔 指 酸 电 离
的.2
4;
:6
<;
9
=(
7
阴离子的放电顺序
是 惰 性 电 极 时 : 4
>
?
4
含 氧 酸 根 离 子 :
4
=;
是活性电极时:电极本身溶解放电
注意先要看电极材料,是惰性电极还是活性电极,假设阳极材料为活性电极
〔:6、8等金属,那么阳极反响为电极材料失去电子,变成离子进入溶液;
假设为惰性材料,那么根据阴阳离子的放电顺序,依据阳氧阴还的规律来书写
电极反响式。
电解质水溶液点解产物的规律
4 / 17
剩余16页未读,继续阅读
资源评论

beibeidzh
- 粉丝: 8
- 资源: 24万+

下载权益

C知道特权

VIP文章

课程特权
开通VIP
上传资源 快速赚钱
 我的内容管理
展开
我的内容管理
展开
 我的资源
快来上传第一个资源
我的资源
快来上传第一个资源
 我的收益 登录查看自己的收益
我的收益 登录查看自己的收益 我的积分
登录查看自己的积分
我的积分
登录查看自己的积分
 我的C币
登录后查看C币余额
我的C币
登录后查看C币余额
 我的收藏
我的收藏  我的下载
我的下载  下载帮助
下载帮助

 前往需求广场,查看用户热搜
前往需求广场,查看用户热搜安全验证
文档复制为VIP权益,开通VIP直接复制
 信息提交成功
信息提交成功
