物理化学实验报告No2蒸气压.doc
需积分: 0 78 浏览量
更新于2010-04-23
收藏 1.1MB DOC 举报
【蒸气压】是指在一定温度下,液体表面产生的蒸汽与其液相达到动态平衡时的蒸气压强。这是液体挥发性的一个重要参数,反映了液体转变为气态的能力。蒸气压与温度有关,温度越高,分子活动越剧烈,液体更容易转变为蒸气,蒸气压也就越大。
【沸点】是指在特定外压下,液体变为气体的温度。对于纯液体,当外界压力等于其饱和蒸气压时,液体就会沸腾,这个温度就是沸点。沸点会随着外压的变化而变化,这就是为什么在高山上煮水的温度会低于海平面的原因。
【饱和蒸气压】是液体在一定温度下,其蒸气压与液相达到平衡时的压力。在这个压力下,液体和蒸汽可以共存,且液体不再继续蒸发,蒸气也不再凝结。本实验中,通过测量不同外压下的沸点,可以得到不同温度下的饱和蒸气压。
【动态法】是测定饱和蒸气压的一种方法,通过改变外部压力并测量对应的沸点,从而得到饱和蒸气压。这种方法相对于静态法和饱和气流法,操作简便,结果较为准确,尤其适用于蒸气压不高的液体,如本实验中的纯水。
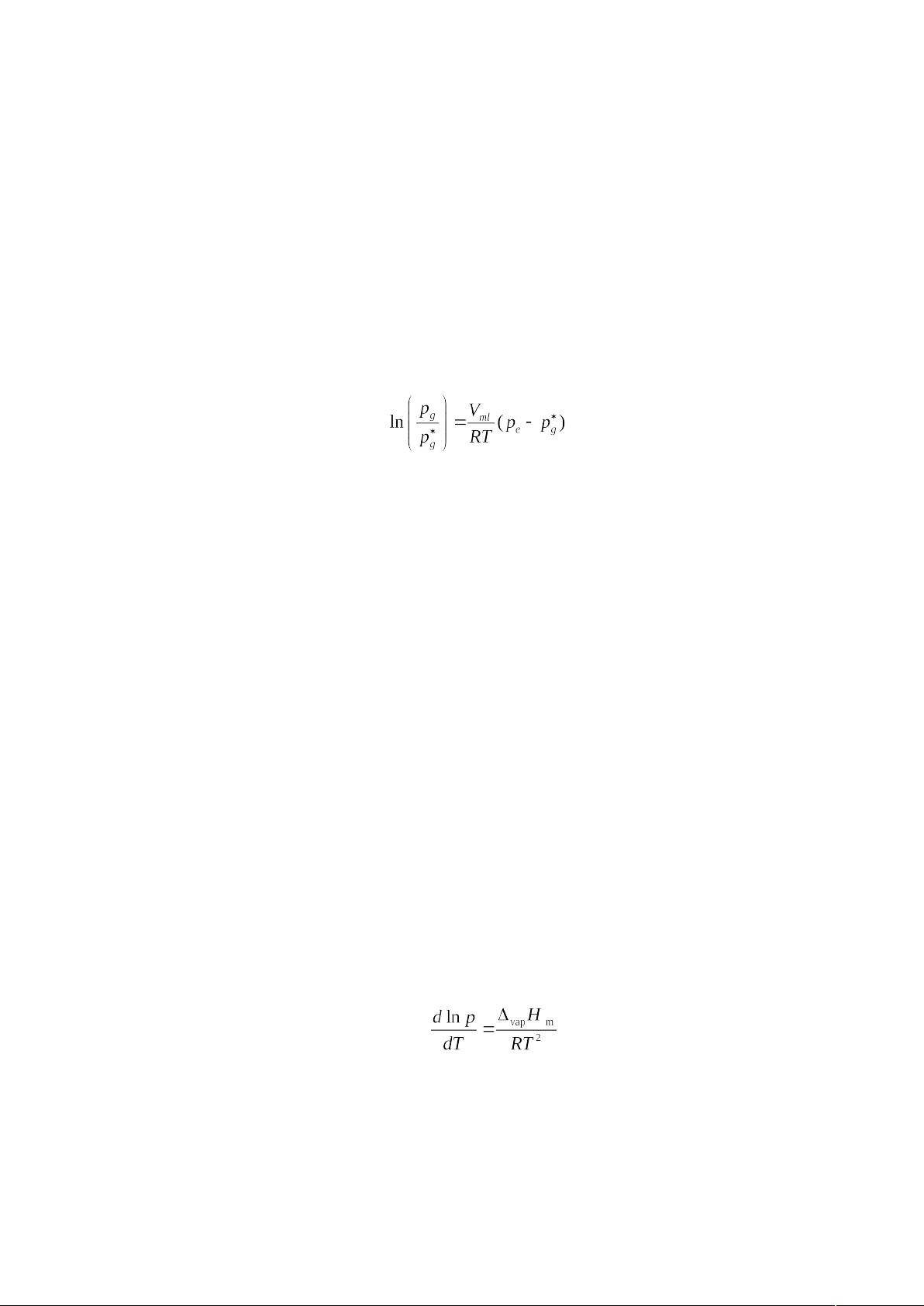
【克拉贝龙-克劳修斯方程】描述了饱和蒸气压、温度和摩尔汽化热之间的关系。根据该方程,可以通过实验得到的数据来计算摩尔汽化热,即每摩尔液体在一定温度下蒸发所需的热量。
【摩尔汽化热】是单位摩尔液体在标准状态下(通常是1大气压)转化为同温同压的蒸气所需的热量。在本实验中,通过对水的饱和蒸气压进行测定,可以推算出水在不同温度下的摩尔汽化热。
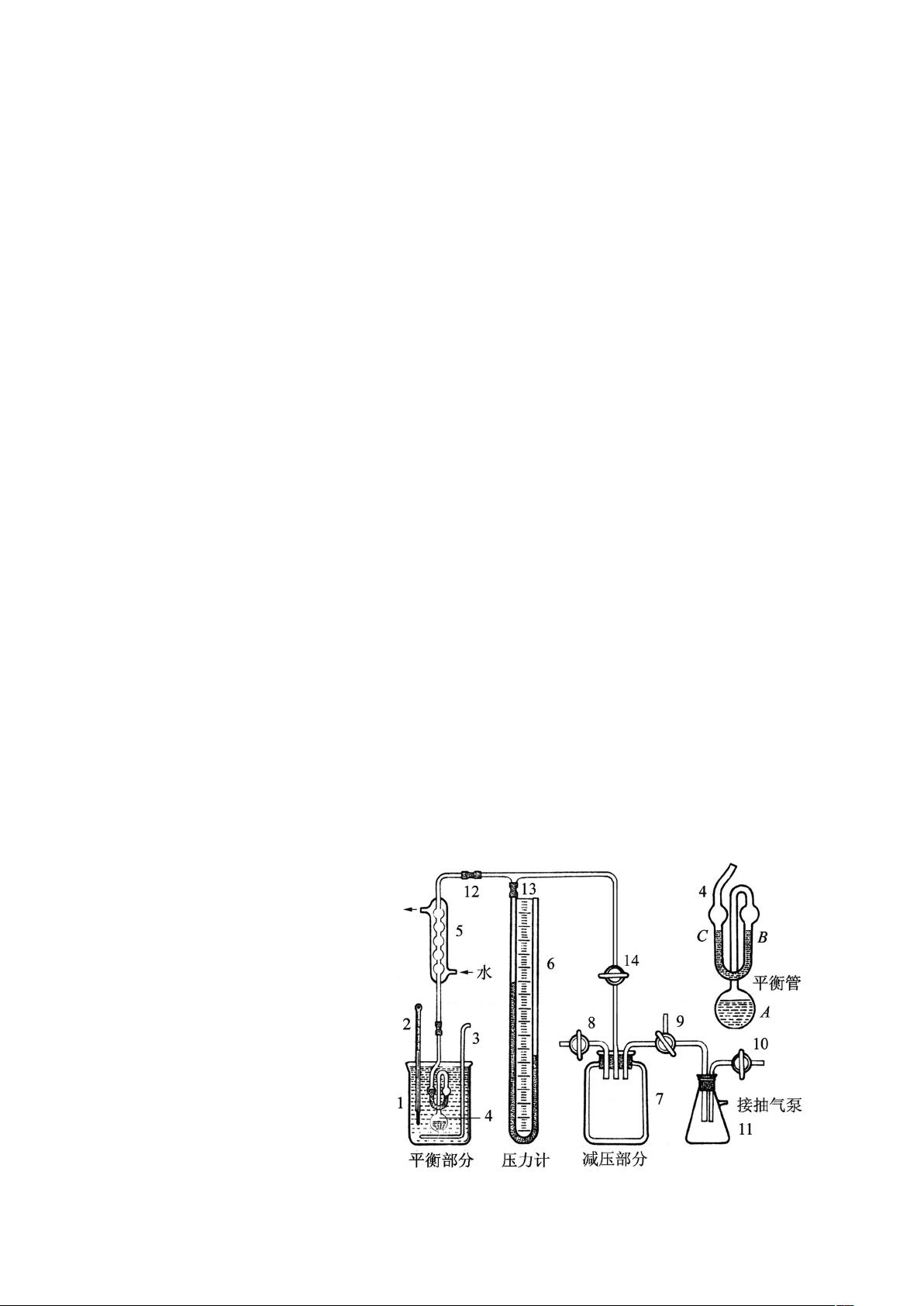
【实验装置】包括U形压力计、旋片真空泵、电动搅拌机、电加热器、大气压计以及各种玻璃器皿等。这些设备用于维持和控制实验过程中的压力、温度和液气平衡状态,以便精确测量蒸气压。
实验步骤中,通过调节外部压力和观察沸点,记录不同压力下对应的温度,然后利用克拉贝龙-克劳修斯方程处理数据,计算出水的饱和蒸气压和摩尔汽化热。在整个过程中,需要注意消除空气的影响,因为空气的存在会降低实际测得的蒸气压。
总结来说,这篇物理化学实验报告主要探讨了如何利用动态法测定纯水的饱和蒸气压,验证了沸点与外压的关系,并通过实验数据应用克拉贝龙-克劳修斯方程求得了水的摩尔汽化热。实验方法的准确性和可操作性为理解和研究物质的蒸气压性质提供了实践基础。
zq521522523
- 粉丝: 0
- 资源: 1
最新资源
- 网络原理课程设计【校园网规划】+思科模拟器,包含pkt文件及完整实验报告,附录含有源码
- 学生公寓管理系统论文+源码(在文档中)
- 风电场参与下的市场竞价策略
- 致远协同 V8.0SP1 数据字典
- Excel数据合并拆分器.zip
- Prime-Series-Level-1.z06
- Prime-Series-Level-1.z04
- Prime_Series_Level-1.z05
- C语言 实现AES-CBC-128-ZeroPadding 加解密算法 完整示例工程 - 基于STM32F103的运行环境,但代码移植性很高
- chromedriver version 118.0.5993.70
- chromedriver.exe-118.0.5993.32、win32/64位、爬虫、自动化测试、Web自动化
- chromedriver.exe-118.0.5993.3、win32/64位、爬虫、自动化测试、Web自动化
- fluent翼型动态前缘下垂,动网格,udf程序实现,俯仰运动同时前缘动态下垂,udf程序代码,fluent case和视频教程 流体力学,船舶海洋,能源动力,航空航天专业必备
- Prime_Series_Level-1.z08
- Prime_Series_Level-1.z07
- Prime_Series_Level-1.z09