没有合适的资源?快使用搜索试试~ 我知道了~
化工流程分类解析word版.doc含答案.doc
1.该资源内容由用户上传,如若侵权请联系客服进行举报
2.虚拟产品一经售出概不退款(资源遇到问题,请及时私信上传者)
2.虚拟产品一经售出概不退款(资源遇到问题,请及时私信上传者)
版权申诉
0 下载量 95 浏览量
2021-10-03
10:53:06
上传
评论
收藏 1.41MB DOC 举报
温馨提示

试读
17页
化工流程分类解析word版.doc含答案.doc
资源推荐
资源详情
资源评论

- .
专题复习---无机化工流程试题〔一〕
例题 1.稀土元素是周期表中 IIIB 族钪、钇和镧系元素的总称,它们都是很活泼的金属,性质极为相似,常见化合
价为+3。我国蕴藏着丰富的钇矿石〔Y
2
FeBe
2
Si
2
O
10
〕,以此矿石为原料生产氧化钇〔Y
2
O
3
〕的主要流程如下:
: ① 有关金属离子形成氢氧化
物 沉 淀时的 pH 如下表:
开场沉淀时的 pH 完全沉淀时的 pH
Fe
3+
2.7 3.7
Y
3+
6.0 8.2
② 在周期表中,铍、铝元素处于第二周期和第三周期的对角线位置,化学性质相似。
〔1〕钇矿石〔Y
2
FeBe
2
Si
2
O
10
〕的组成用氧化物的形式可表示为。
〔2〕欲从 Na
2
SiO
3
和 Na
2
BeO
2
的混合溶液中制得 Be(OH)
2
沉淀。那么
① 最好选用盐酸、〔填字母〕两种试剂,再通过必要的操作即可实现。
a.NaOH 溶液 b.氨水 c.CO
2
气 d.HNO
3
② 写出 Na
2
BeO
2
与足量盐酸发生反响的离子方程式:。
〔3〕沉淀 A 为〔填化学式〕;
为使 Fe
3+
沉淀完全,须用氨水调节 pH =a,那么 a 应控制在的围;
检验 Fe
3+
是否沉淀完全的操作方法是。
例题 2.工业上制取 CuCl
2
的生产流程如下:
请结合下表数据,答复以下问题:
物 质
Fe(OH)
2
Cu(OH)
2
Fe(OH)
3
溶度积/25℃ 8.0×10
-
16
2.2×10
-
20
4.0×10
-
38
完全沉淀时的 pH 围
≥9.6 ≥6.4
3~4
〔1〕写出以下主要离子方程式:
A→B; B→C+D。
〔2〕溶液 A 中参加 NaClO 的目的是。
〔3〕在溶液 B 中参加 CuO 的作用是。
〔4〕操作①应控制的 pH 围是:;操作②的目的是。
〔5〕由 Cu(OH)
2
参加盐酸使 Cu(OH)
2
转变为 CuCl
2
。采用“稍多量盐酸〞和“低温蒸干〞的目的是 。
例题 3.二氧化锰是制造锌锰干电池的根本材料。工业上以软锰矿为原料,利用硫酸亚铁制备高纯
- .word.zl.
- .
二氧化锰的流程如下:
某软锰矿的主要成分为 MnO
2
,还含有 Si〔16.72%〕、Fe〔5.86%〕、Al〔3.42%〕、Zn〔2.68%〕和
Cu〔0.86%〕等元素的化合物。局部阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的
pH 见下表,答复以下问题:
沉淀物
Al(OH
)
3
Fe(OH
)
3
Fe(OH
)
2
Mn(O
H)
2
Cu(OH
)
2
Zn(OH
)
2
CuS ZnS MnS FeS
pH 5.2 3.2 9.7 10.4 6.7 8.0 ≥–0.42 ≥2.5 ≥7 ≥7
〔1〕硫酸亚铁在酸性条件下将 MnO
2
复原为 MnSO
4
,酸浸时发生的主要反响的化学方程
式为
〔2〕滤渣 A 的主要成分是。
〔3〕参加 MnS 的目的是除去杂质。
〔4〕碱性锌锰电池中总反响式:Zn+2MnO
2
+2H
2
O = 2MnOOH+Zn(OH)
2
MnO
2
参与的电极反响方程式为。
〔5〕从废旧碱性锌锰电池中可以回收利用的物质有〔写出两种〕。
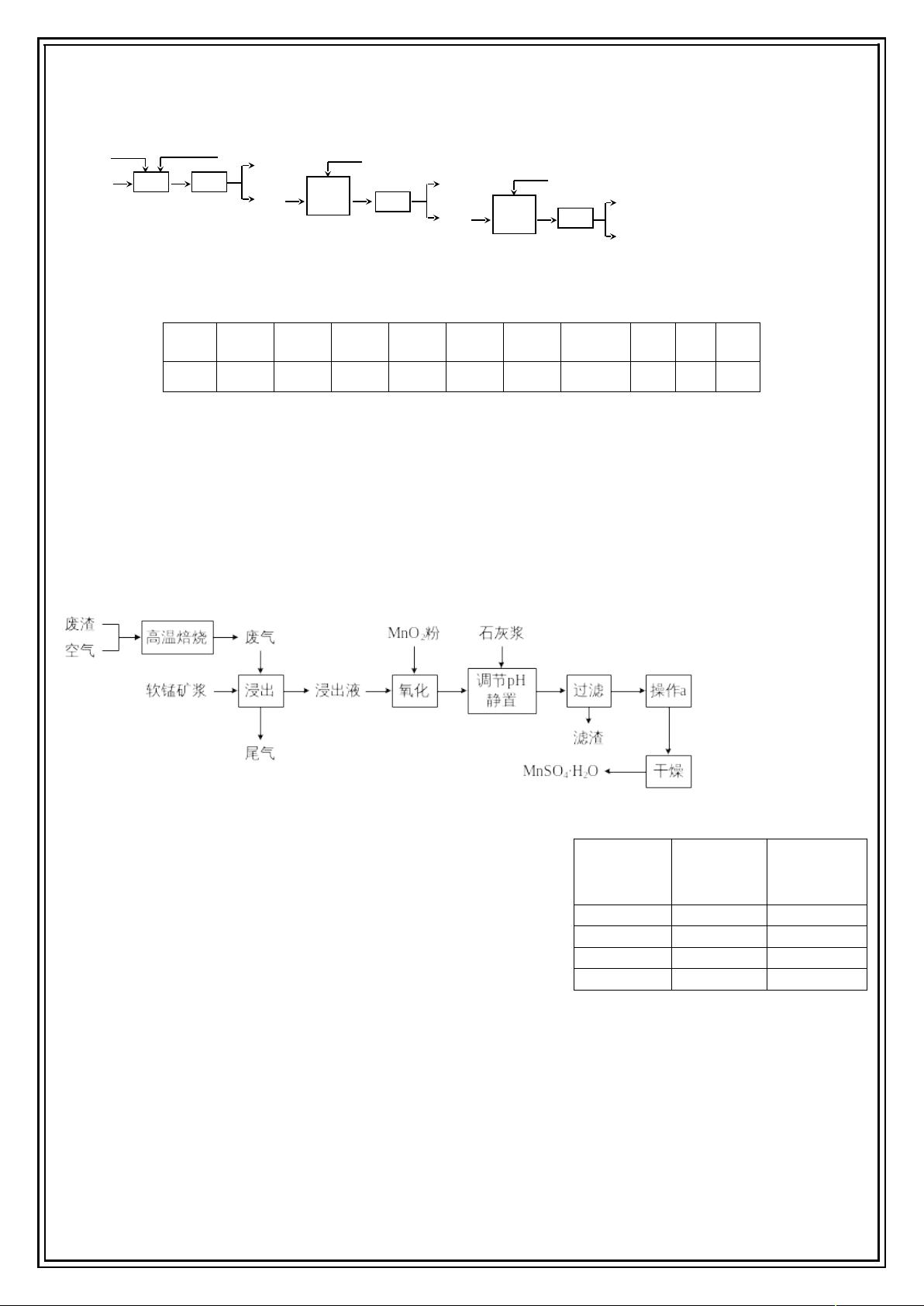
例题4.为了回收利用SO
2
,研究人员研制了利用低品位软锰矿浆〔主要成分是MnO
2
〕吸收高温焙烧含硫废渣产生
的SO
2
废气,制备硫酸锰晶体的生产流程,其流程示意图如下:
,浸出液的 pH<2,其中的金属离子主要是 Mn
2
+
,还含有少量的 Fe
2
+
、Al
3
+
等金属离子;有关金属离子形成氢
氧化物沉淀时的 pH 见右表。请答复以下问题:
〔1〕浸出过程中主要反响的化学方程式为
。
〔2〕氧化过程中主要反响的离子方程式为
。
〔3〕在氧化后的液体中参加石灰浆是用于调节pH〔设溶液中离
子浓度≥0.01mol/L〕,那么pH应调节至。
〔4〕滤渣的主要成分的化学式为。
〔5〕以下各组试剂中,能准确测定尾气中SO
2
含量的是__________〔填编号〕。
a. NaOH溶液、酚酞试液b. 稀H
2
SO
4
酸化的KMnO
4
溶液
c. 碘水、淀粉溶液d. 氨水、酚酞试液
练习:
1. 胆矾〔五水硫酸铜〕是一种常见的化合物,工业上它也是一种制取其它含铜化含物的原料。
- .word.zl.
离子
(0.01mo/
L)
开场
沉淀的pH
完全
沉淀的pH
Fe
2
+
7.5 9.7
Fe
3
+
2.2 3.2
Al
3
+
4.0 5.2
Mn
2
+
8.6 10.4
软锰矿 酸浸
H
2
SO
4
过量 FeSO
4
过滤
滤渣
滤液
液
调 pH
至 5.4
氨水
液
过滤
滤渣 A
滤液
液
加热至
沸
MnS
液
过滤
滤渣
滤液
液
→ … → 高 纯
MnO
2
液
趁热过滤
煮沸数分钟
参加 Zn 粉
滤渣 III
滤渣 II
滤液 II
滤液 III 晶体
调 pH 至 5-5.4
参加 ZnO
酸性 KMnO
4
混合液
趁热过滤
粗产品
酸浸
滤渣 I
滤液 I
- .
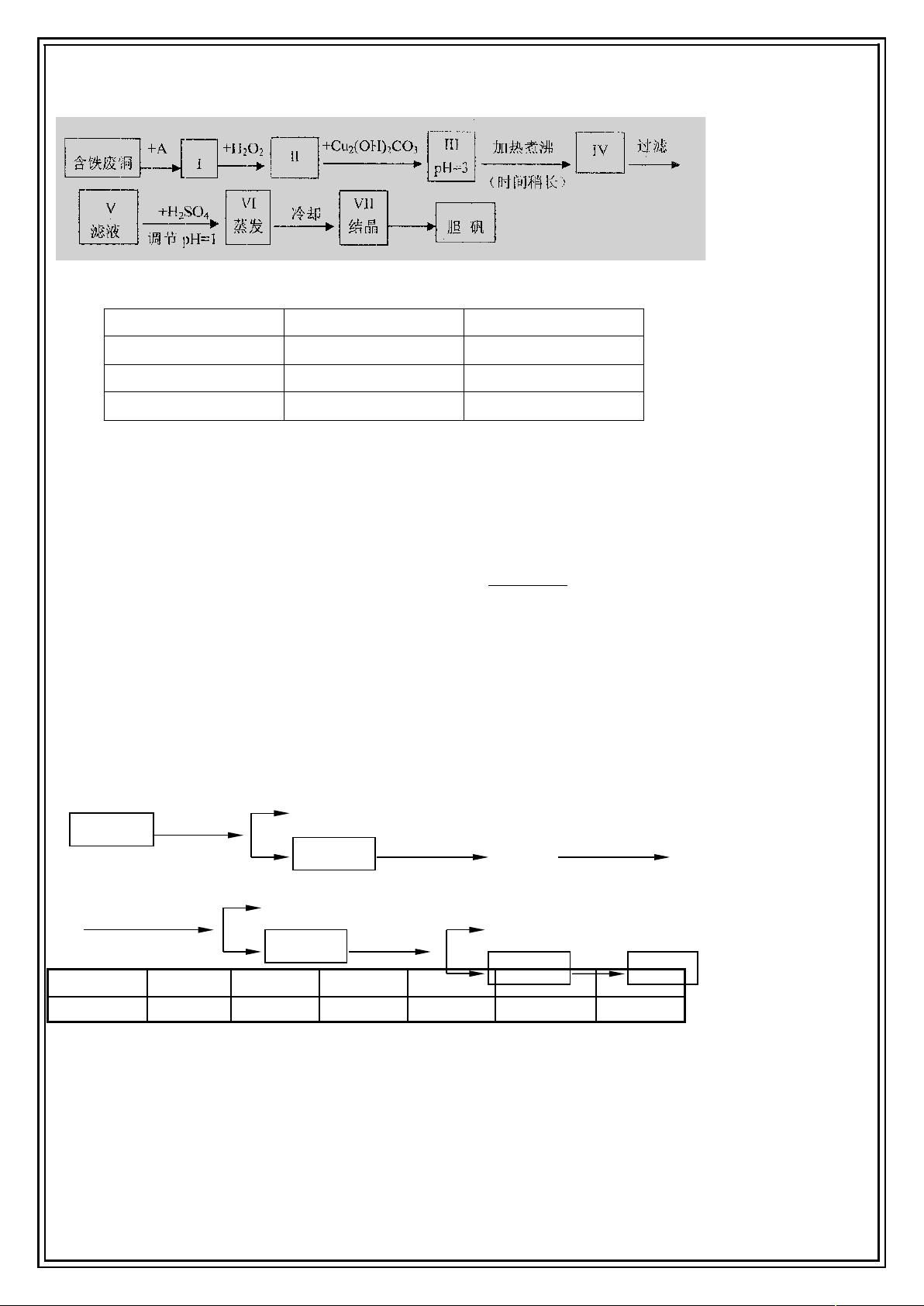
现有废铜〔主要杂质为 Fe〕来制备胆矾。有人设计了如下流程:
pH 控制可参考以下数据
物质 开场沉淀时的 pH 完全沉淀对的 pH
氢氧化铁 2.7 3.7
氢氧化亚铁 7.6 9.6
氢氧化铜 5.2 6.4
请根据上述流程答复以下问题:
〔1〕A 物质可选用 。〔填字母〕。
a.稀 H
2
SO
4
b.浓 H
2
SO
4
/△ c.浓 FeC1
3
溶液 d.浓 HNO
3
写出 A 物质溶解铜的化学方程式
〔2〕I 中加 H
2
O
2
的目的。
〔3〕II 中也可以参加以下物质中的代替 Cu
2
〔OH〕
2
CO
3
〔 填字母〕。
A.NH
3
B.CuO C.NaOH D.Na
2
CO
3
E.Cu〔OH〕
2
〔4〕Ⅲ加热煮沸时发生的化学反响的离子方程式为。
25℃时 Fe〔OH〕
3
的溶度积为 2.6×10
-39
,试计算 25℃时,用溶液中 Fe
3+
的浓度为
〔5〕IV 过滤所需要的玻璃仪器除烧杯外还有。
〔6〕V 中加 H
2
SO
4
调节 pH=1 是为了。
〔7〕某工程师认为上述流程中所加的 A 物质并不理想,需作改进,其理由是。
2.从粗产品硫酸锌固体除去铁、铜、镉等可溶性硫酸盐,从而得到纯洁的硫酸锌,实验流程如下:
局部阳离子以氢氧化物形式完全沉淀时溶液的 pH 参见上表,请答复以下问题:
〔1〕“酸浸〞步骤中,为提高锌的浸出率,可采取的措施有。“酸浸〞时适当补充少量水的原因是。
〔2〕滤液 I 参加酸性 KMnO
4
所发生反响的离子方程式为。
参加 ZnO 的原因是。
〔3〕滤渣 III 的成份主要是。
〔4〕从滤液 III 得到晶体的操作过程为 、冷却结晶、过滤冼涤、小心枯燥。
3. 回收的废旧锌锰于电池经过处理后得到锰粉(含 MnO
2
、Mn(OH)
2
、Fe、NH
4
Cl 和炭黑等),由锰粉制取 MnO
2
- .word.zl.
沉淀物
Zn(OH)
2
Fe(OH)
2
Fe(OH)
3
Cu(OH)
2
Cd(OH)
2
Mn(OH)
2
pH 值
8.0 9.7 3.2 6.7 9.4 10.4

- .
的步骤如以下列图所示:
根据上图所示步骤并参考左边表格数据答复以下问题:
〔1〕在加热条件下用浓盐酸浸取锰粉,所得溶液中含有 Mn
2+
、Fe
2+
等。MnO
2
与浓盐酸反响的离子方程式为;
这种处理方法缺乏之处为:。
〔2〕锰粉经浓盐酸浸取,过滤 I 除去不溶杂质后,向滤液中参加足量 H
2
O
2
溶液,其作用是___________________
______。
〔3〕过滤 I 的滤渣的化学式为;过滤Ⅱ的滤渣的化学式为。
〔4〕将过滤 I 所得滤液经 H
2
O
2
氧化后,再参加 NaOH 溶液调节 pH 的围是:,其目的是。
〔5〕过滤Ⅱ所得滤液参加足量 H
2
O
2
溶液并参加 NaOH 溶液调节 pH 约为 9,使 Mn
2+
氧化得到 MnO
2
,反响的离
于方程式为__________________________________________。
4.碳酸锂广泛应用于瓷和医药等领域。已 -锂辉石〔主要成分为 Li
2
O Al
2
O
3
4SiO
2
〕为原材料制备 Li
2
CO
3
的工
艺流程如下:
: Fe
3+
、 Al
3+
、 Fe
2+
和 Mg
2+
以 氢 氧 化 物 形 式 完 全 沉 淀 时 , 溶 液 的 PH 分 别 为 3.2 、 5.2 、 9.7 和 12.4 ;
Li
2
SO
4
、LiOH 和 Li
2
CO
3
在 303K 下的溶解度分别为 34.2g、12.7g 和 1.3g.
〔1〕步骤Ⅰ前,B-锂辉石要粉碎成细颗粒的目的是_____________.
〔2〕步骤Ⅰ中,酸浸后得到的酸性溶液中含有 Li
+
、SO
4
2-
,另含有 Al
3+
、Fe
3+
、Fe
2+
、Mg
2+
、Ca
2+
、Na
+
等杂质,
需在搅拌下参加_____________(填“石灰石〞、“氯化钠〞或“稀硫酸〞)以调节溶液的 PH 到 6.0~6.5,沉淀局部杂
质离子,然后别离得到浸出液。
〔3〕步骤Ⅱ中,将适量的 H
2
O
2
溶液、石灰乳和 Na
2
CO
3
溶液依次参加浸出液中,可除去的杂质金属离子有_____
_________.
〔4〕步骤Ⅲ中,生成沉淀的离子方程式为________________.
〔5〕从母液中可回收的主要物质是___________.
专题复习---无机化工流程试题〔二〕
例题 1.锂离子电池的广泛应用使回收利用锂资源成为重要课题:其中需要重点回收的是正极材料,其主要成分为
- .word.zl.
剩余16页未读,继续阅读
资源评论

wdqsv88
- 粉丝: 4
- 资源: 13万+

下载权益

C知道特权

VIP文章

课程特权
开通VIP
上传资源 快速赚钱
 我的内容管理
展开
我的内容管理
展开
 我的资源
快来上传第一个资源
我的资源
快来上传第一个资源
 我的收益 登录查看自己的收益
我的收益 登录查看自己的收益 我的积分
登录查看自己的积分
我的积分
登录查看自己的积分
 我的C币
登录后查看C币余额
我的C币
登录后查看C币余额
 我的收藏
我的收藏  我的下载
我的下载  下载帮助
下载帮助

 前往需求广场,查看用户热搜
前往需求广场,查看用户热搜安全验证
文档复制为VIP权益,开通VIP直接复制
 信息提交成功
信息提交成功
