没有合适的资源?快使用搜索试试~ 我知道了~
锂离子电池及其它新型电池专题.doc
1.该资源内容由用户上传,如若侵权请联系客服进行举报
2.虚拟产品一经售出概不退款(资源遇到问题,请及时私信上传者)
2.虚拟产品一经售出概不退款(资源遇到问题,请及时私信上传者)
版权申诉
0 下载量 57 浏览量
2022-12-09
18:03:39
上传
评论
收藏 959KB DOC 举报
温馨提示

试读
21页
锂离子电池及其它新型电池专题.doc
资源推荐
资源详情
资源评论

1
锂离子电池及其它新型电池专题
1.市场上经常见到的标记为 Li-ion 的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料
(碳作为金属锂的载体),电解质为一种能传导 Li 的高分子材料。这种锂离子电池的电池反应为:
Li+2Li
下列说法不正确的是
A.放电时,负极的电极反应式:Li-e =Li
B.充电时,Li 既发生氧化反应又发生还原反应
C.该电池不能用水溶液作为电解质
D.放电过程中 Li 向负极移动
答案 D
【解析】A 项,Li 从零价升至正价,失去电子,作为负极,正确;B 项,反应逆向进行时。反应物只有一种,
故化合价既有升,又有降,所以既发生氧化反应又发生还原反应,正确;C 项,由于 Li 可以与水反应,故应
为非水材料,正确;D 项,原电池中阳离子应迁移至正极失电子,故错。
2. 以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是
A.该电池能够在高温下工作
B.电池的负极反应为:
C.放电过程中, 从正极区向负极区迁移
D.在电池反应中,每消耗 1mol 氧气,理论上能生成标准状况下 气体
【标准答案】B
【解析】A 项,高温条件下微生物会变性,所以 A 错;B 项,负极是葡萄糖失电子生成二氧化碳,所以 B 对;
C 项,原电池内部阳离子应向正极移动,所以 C 错;D 项,消耗 1mol 氧气生成 1mol 二氧化碳,标准状况下
体积是 22.4L,D 错。
【考点分析】
①原电池反应(反应原理、电极方程式的书写、离子的移动方向);②有关化学方程式的计算。
2.氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小
的铂粉,铂吸附气体的能力强,性质稳定,请回答:
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为
(用 a、b 表示)。
(2)负极反应式为 。
(3)电极表面镀铂粉的原因为 。
(4)该电池工作时,H
2
和 O
2
连续由外部供给,电池可连续不断提供电能。因此,大量安全
储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H
2
2LIH
Ⅱ.LiH+H
2
O==LiOH+H
2
↑
①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
②已知 LiH 固体密度为 0.82g/cm
3
。用锂吸收 224L(标准状况)H
2
,生成的 LiH 体积与被吸收的 H
2
体积比
为 。
③由②生成的 LiH 与 H
2
O 作用,放出的 H
2
用作电池燃料,若能量转化率为 80%,则导线中通过电子的物质的
量为 mol。
+
0.35 2 0.85 2
2NiO Li NiO
¾ ¾ ¾®
¬ ¾ ¾¾
放电
充电
-
+
0.85 2
NiO
+
- +
6 12 6 2 2
C H O +6H O-24e =6CO +24H�
+
H
2
CO
22.4
6
L
�

2
③32
【解析】本题考查电化学知识。(1)原电池的实质为化学能转化成电能。总反应为 2H
2
+ O
2
=2H
2
O,其中 H
2
从零价升至+1 价,失去电子,即电子从 a 流向 b。(2)负极为失去电子的一极,即 H
2
失电子生成 H
+
,由于
溶液是碱性的,故电极反应式左右应各加上 OH
-
。(3)铂粉的接触面积大,可以加快反应速率。(4)I.Li 从
零价升至+1 价,作还原剂。II.H
2
O 的 H 从+1 降至 H
2
中的零价,作氧化剂。由反应 I,当吸收 10molH
2
时,则
生成 20molLiH,V=m/ρ=20×7.9/0.82 ×10
-3
L=192.68×10
-3
L。
V
(LiH)/v(H
2
)= 192.68×10
-3
L/224L=8.71×
10
-4
。20mol LiH 可生成 20mol H
2
,实际参加反应的 H
2
为 20×80%=1.6mol,1molH
2
转化成 1molH
2
O,转移 2mol
电子,所以 1.6molH
2
可转移 3.2mol 的电子。
3.新型锂离子电池在新能源的开发中占有重要地位。可用作节能环保电动汽车的动力电池。磷酸亚铁锂
(LiFePO
4
)是新型锂离子电池的首选电极材料,它的制备方法如下:
方法一:将碳酸锂、乙酸亚铁[(CH
3
COO)
2
Fe]、磷酸二氢铵按一定比例混合、充分研磨后,在 800℃左右、
惰性气体氛围中煅烧制得晶态磷酸亚铁锂,同时生成的乙酸及其它产物均以气体逸出。
方法二:将一定浓度的磷酸二氢铵、氯化锂混合溶液作为电解液,以铁棒为阳极,石墨为阴极,电解析出磷
酸亚铁锂沉淀。沉淀经过滤、洗涤、干燥,在 800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂。
在锂离子电池中,需要一种有机聚合物作为正负极之间锂离子选移的介质,该有机聚合物的单体之一(用 M
表示)的结构简式如下:
请回答下列问题:
(1)上述两种方法制备磷酸亚铁锂的过程都必须在惰性气体氛围中进行。其原因是
。
(2)在方法一所发生的反应中,除生成磷酸亚铁锂、乙酸外,还有 、
、 (填化学式)生成。
(3)在方法二中,阳极生成磷酸亚铁锂的电极反应式为
。
(4)写出 M 与足量氧化钠溶液反应的化学方程式:
。
(5)已知该锂离子电池在充电过程中,阳极的磷酸亚铁锂生成磷酸铁,则该电池放电时正极的电极反应式为
。
答案.(15 分)
(1)为了防止亚铁化合物被氧化
(2)CO
2
H
2
O NH
3
(每空 1 分,共 3 分)
(3)Fe+H
2
P
4
O
-
+Li
+
-
2e
-
=LiFePO
4
+2H
+
(3 分)
(4)

3
(3 分)
(5)FePO
4
+Li
+
+e
-
====LiFePO
4
(3 分)【解析】(1)亚
铁离子具有强还原性,制备磷酸亚铁锂的过程都必须在惰性气体氛围中进行。其原因是为了防止亚铁化合物
被氧化(2)将碳酸锂、乙酸亚铁、磷酸二氢铵在 800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂、乙
酸及其它产物均以气体逸出。根据题意和元素守恒,可得其他产物为:CO
2
、H
2
O 和 NH
3
。(3)将一定
浓度的磷酸二氢铵、氯化锂混合溶液作为电解液,以铁棒为阳极,石墨为阴极,电解析出磷酸亚铁锂沉淀。
阳极生成磷酸亚铁锂的电极反应式为 Fe+H
2
P
4
O
-
+Li
+
-
2e
-
=LiFePO
4
+2H
+
(4) M 具有酯基,在碱性条件
下 可 发 生 水 解 , M 与 足 量 氧 化 钠 溶 液 反 应 的 化 学 方 程 式 :
【考点分析】氧化还原、电极方程式、有机化学方程式综合运用
4. Li-SOCl
2
电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是 LiAlCl
4
—SOCl
2
。电池的
总反应可表示为:4Li+2SOCl
2
= 4LiCl +S +SO
2
。
请回答下列问题:
(1)电池的负极材料为 ,发生的电极反应为 ;
(2)电池正极发生的电极反应为 ;
(3)SOCl
2
易挥发,实验室中常用 NaOH 溶液吸收 SOCl
2
,有 Na
2
SO
3
和 NaCl 生成。 如果把少量水滴到
SOCl
2
中,实验现象是 ,反应的化学方程式为 ;
(4)组装该电池必须在无水、无氧的条件下进行,原因是 。
答案(1)负极材料为 Li(还原剂),Li – e
-
= Li
+
(2)2SOCl
2
+ 4 e
-
= 4Cl
-
+ S + SO
2
(3)出现白雾,有刺激性气体生成 SOCl
2
+ H
2
O = SO
2
↑+ 2HCl↑
(4)因为构成电池的两个主要成份 Li 能和氧气水反应,且 SOCl
2
也与水反应
【解析】分析反应的化合价变化,可得 Li 为还原剂 ,SOCl
2
为氧化剂。
(1)负极材料为 Li(还原剂),Li – e
-
= Li
+
(2)负极反应式可由总反应减去负极反应式得到:2SOCl
2
+ 4 e
-
= 4Cl
-
+ S + SO
2
(3)题中给出有碱液吸收时的产物,则没有碱液吸收时的产物应为 SO
2
和 HCl,所以现象应该为出现白雾和
有刺激性气体生成。
(4)因为构成电池的两个主要成份 Li 能和氧气水反应,且 SOCl
2
也与水反应
4
、镍镉(
Ni-Cd
)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为
KOH
溶液,其充、
放电按下式进行:
Cd + 2NiOOH + 2H
2
O
·Åµç
³ä µç
Cd(OH)
2
+ 2Ni(OH)
2
有关该电池的说法正确的是(
)
A.充电时阳极反应:Ni(OH)
2
-e
—
+ OH
-
== NiOOH + H
2
O
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
4
D.放电时电解质溶液中的 OH
-
向正极移动
解析:由充电时方程式中的
Cd
和
Ni
的化合价的变化可知,
Ni(OH)
2
作阳极,电解质溶液为
KOH
,所以电极
反应式为:
Ni(OH)
2
-
e
-
+
OH-
===
NiOOH
+
H
2
O
;
Cd(OH)
2
作阴极,
Cd(OH)
2
+
2e
-
===
Cd
+
2OH
-
;
充电的过程是将电能转化为化学能,放电时,
Cd
作负极,
Cd
-
2e
-
+
2OH
-
===
Cd(OH)
2
,
Cd
周围的
c(OH
-
)
下降,
OH
-
向负极移动。
答案:
A
。
5 、LiFePO
4
电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电池反应为:FePO
4
+Li
放电
充电
LiFePO
4
,电池的正极材料是 LiFePO
4
,负极材料是石墨,含 U 导电固体为电解质。下列有关 LiFePO
4
电池说法正确的是
A.可加入硫酸以提高电解质的导电性
B 放电时电池内部 Li 向负极移动.
C.充电过程中,电池正极材料的质量减少
D.放电时电池正极反应为:FePO
4
+Li
+
+e
-
=LiFePO
4
解析: 16CD 解释: 放电时,负极:Li -- e- ==Li+,正极:FePO4 + Li+ + e- == LiFePO4;充电时,阳极:
LiFePO4 -- e- == FePO4 + Li+ 阴极:Li+ + e- == Li,所以易知 C.D 正确。
若加入硫酸,与 Li 单质(固体)发生反应,所以 A 错;放电时,Li+应(正电荷)在电池内部(电解质中)
向正极移动,故 B 错。
16.一定条件下,电解较稀浓度的硫酸,其还原产物为双氧水,该原理可用于制取双氧水,其电解的化学方程
式为:3H
2
O+ 3O2 =O3 + 3H
2
O 。下列有关说法正确的是( )C
A、电解池的阳极生成双氧水,阴极生成臭氧
B、电解池中硫酸溶液的 pH 保持不变
C、产生臭氧的电极反应式为 3H
2
O —6e—= O3 + 6H+
D、产生双氧水的电极反应式为 2H
2
O —2e —=H
2
O
2
+ 2H+
6、一种新型熔融盐燃料电池具有高发电效率。现用 Li2CO3 和 Na2CO3 的熔融盐混合物作电解质,一极通 CO
气体,另一极通 O2 和 CO
2
混合气体,其总反应为:2CO+ O2 == 2CO
2
。则下列说法中正确的是()C
A、通 CO 的一极是电池的正极
B、负极发生的电极反应是:O2 + 2CO
2
+ 4e— === 2CO
3
2—
C、负极发生的电极反应是:CO + 2CO
3
2—
—2 e— ===2CO
2
D、正极发生氧化反应
7、用惰性电极电解 CuSO4 溶液。若阴极上析出 Cu 的质量为 3.2g ,则阳极上产生的气体在标准状况下的体
积为 ;常温下,若将电解后的溶液稀释至 1L,则溶液的 pH 约为 。(0.56L;1)
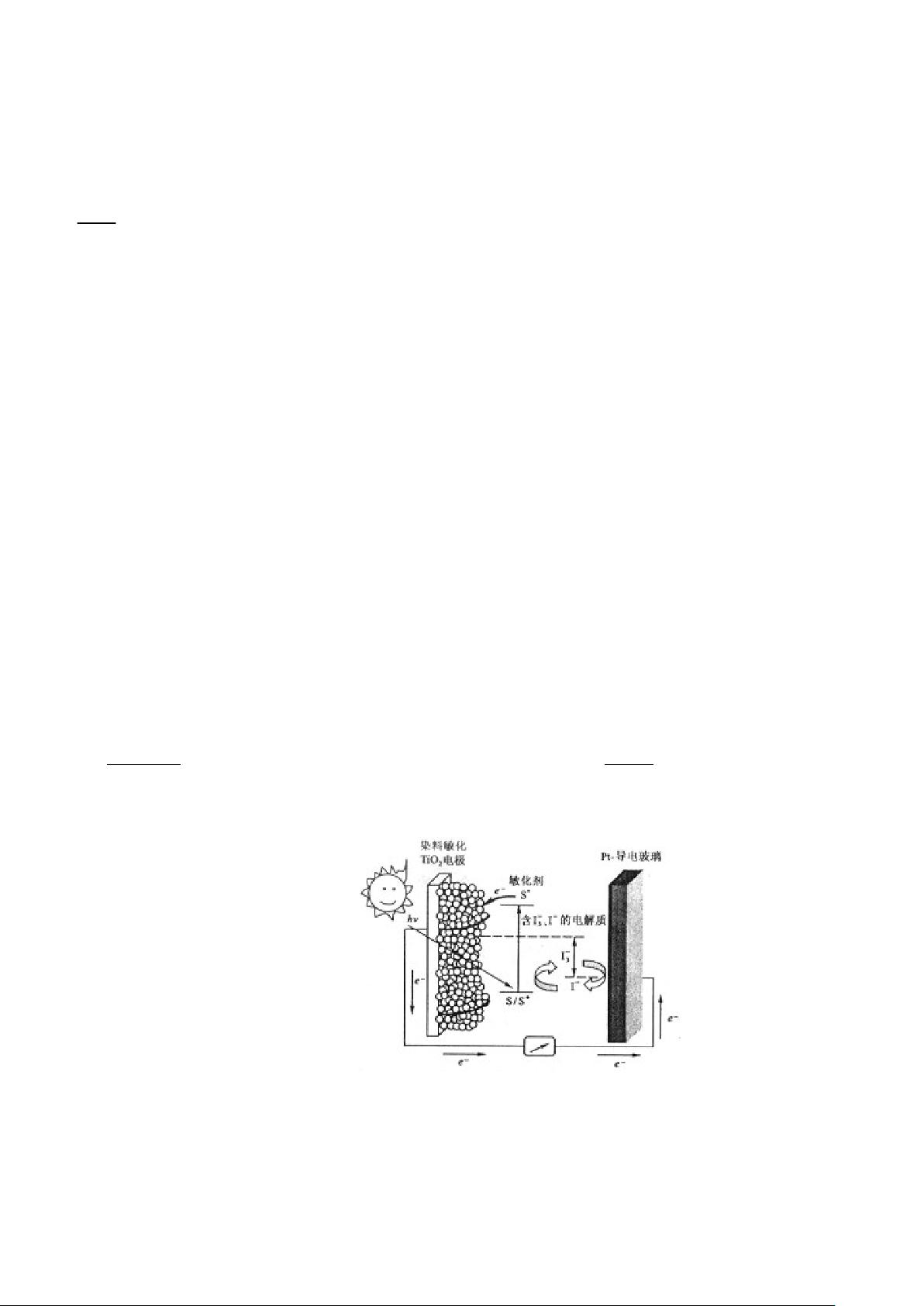
8、(2010 全国 I,10).右图是一种染料敏化太阳能电池的示意图。电池的一个点极由有机光敏燃料(S)
涂覆在
2
TiO
纳米晶体表面制成,另一电极由导电玻璃镀铂构成,电池中发生的反应为:
2 2
TiO /S TiO /S
h
n
*
¾ ¾®
(激发态)
+ -
2 2
TiO /S TiO /S +e
*
¾ ¾®
3
I +2e 3I
- - -
¾ ¾®
2 2 3
2TiO /S 3I 2TiO /S+I
+ - -
+ ¾ ¾®
下列关于该电池叙述错误的是:
A.电池工作时,是将太阳能转化为电能
B.电池工作时,
I
-
离子在镀铂导电玻璃电极上放电
C.电池中镀铂导电玻璃为正极

5
D.电池的电解质溶液中 I
-
和 I
3
-
的浓度不会减少
【解析】B 选项错误,从示意图可看在外电路中电子由负极流向正极,也即镀铂电极做正极,发生还原
反应:I
3
-
+2e
-
=3I
-
;A 选项正确,这是个太阳能电池,从装置示意图可看出是个原电池,最终是将光能转化为
化学能,应为把上面四个反应加起来可知,化学物质并没有减少;C 正确,见 B 选项的解析;D 正确,此太
阳能电池中总的反应一部分实质就是:I
3
-
3I
-
的转化(还有 I
2
+I
-
I
3
-
),另一部分就是光敏有机物从
激发态与基态的相互转化而已,所有化学物质最终均不被损耗!
【答案】B
【命题意图】考查新型原电池,原电池的两电极反应式,电子流向与电流流向,太阳能电池的工作原理,
原电池的总反应式等,还考查考生变通能力和心理素质,能否适应陌生的情境下应用所学知识解决新的问题
等
【点评】本题立意很好,但是考查过为单薄,而且取材不是最新的,在 3 月份江苏省盐城市高三第二次
调研考试化学试题第 17 题(3)问,与此题极为相似的模型,这对一些考生显得不公平!
9、 Li-Al/FeS 电池是一种正在开发的车载电池,该电池中正极的电极反应式为:
有关该电池的下列说法中,正确的是( B)
A、Li-Al 在电池中作为负极材料,该材料中 Li 的化合价为+1 价
B、该电池的电池反应式为:2Li+FeS=Li
2
S+Fe
C、负极的电极反应式为 Al-3 =Al
3+
D、充电时,阴极发生的电极反应式为:
10 、(12 分 )(1) 氢氧燃料电池汽车作为上海世博园中的交通工具之一,下列有关说法不正确的是
________.
A.太阳光催化分解水制氢气比电解水制氢气更为科学
B.氢氧燃料电池作为汽车动力更能保护环境
C.以稀 H
2
SO
4
、KOH 为介质的氢氧燃料电池的负极电极反应式相同
D.以稀 H
2
SO
4
、KOH 为介质的氢氧燃料电池的总反应式相同
(2) 纯电动车采用了高效耐用的一种新型可充电电池,该电池的总反应式为:3Zn +2K
2
FeO
4
+8H
2
O
�
�
�
�
放
电
充
电
3Zn(OH)
2
+2Fe(OH)
3
+4KOH.
①该电池放电时负极反应式为________________.
② 放 电 时 每 转 移 3 mol 电 子, 正 极 有________ mol K
2
FeO
4
被还
原.
(3)锰酸锂离子电池在混合动力车等大型蓄电池应用领域 占 据 主 导 地
位.电池反应式为:Li
1-x
MnO
4
+Li
x
�
�
�
�
放
电
充
电
LiMnO
4
,下列有 关说法不正确
的是________.
A.放电时电池的正极反应式为:Li
1-x
MnO
4
+xLi
+
+xe
-
===LiMnO
4
B.放电过程中,石墨没有得失电子
C.该电池也能在 KOH 溶液的环境中正常工作
D.充电时电池上标有“-”的电极应与外接电源的负极相连
解析:(1)选项 A,电解获得 H
2
消耗较多的能量,而在催化剂作用下利用太阳能来分解 H
2
O 获得 H
2
更
为科学.选项 B,氢氧燃料电池中生成物为 H
2
O,对环境无污染.选项 C,以稀 H
2
SO
4
为介质的电池负极反
应式为:H
2
-2e
-
===2H
+
,以 KOH 为介质的电池负极反应式为 H
2
+2OH
-
-2e
-
===2H
2
O..选项 D,氢氧燃
料电池的总反应式均为:2H
2
+O
2
===2H
2
O.
(2)①放电时,在碱性条件下,负极反应式为:Zn-2e
-
+2OH
-
===Zn(OH)
2
.
②根据电池总反应式可知,2 mol K
2
FeO
4
被还原时有 6 mol 电子转移,所以放电时每转移 3 mol 电子,
有 1 mol K
2
FeO
4
被还原.
(3)选项 A,根据总反应式可知 Li 失去电子,电池负极反应式为:xLi-xe
-
===xLi
+
,由总反应式减去负
极反应式可得放电时的正极反应式为 Li
1-x
MnO
4
+xLi
+
+xe
-
===LiMnO
4
.选项 B,根据总反应式可判断石墨
没有得失电子.选项 C,Li 能与 KOH 溶液中的 H
2
O 反应,导致电池无法正常工作.选项 D,充电过程是放
+
2
2Li +FeS+2e Li Fe
-
= +
e
-
2
Li s+Fe-2 2e Li FeS
- +
= +
氧化
还原
剩余20页未读,继续阅读
资源评论

猫一样的女子245
- 粉丝: 94
- 资源: 2万+

下载权益

C知道特权

VIP文章

课程特权
开通VIP
上传资源 快速赚钱
 我的内容管理
展开
我的内容管理
展开
 我的资源
快来上传第一个资源
我的资源
快来上传第一个资源
 我的收益 登录查看自己的收益
我的收益 登录查看自己的收益 我的积分
登录查看自己的积分
我的积分
登录查看自己的积分
 我的C币
登录后查看C币余额
我的C币
登录后查看C币余额
 我的收藏
我的收藏  我的下载
我的下载  下载帮助
下载帮助

 前往需求广场,查看用户热搜
前往需求广场,查看用户热搜安全验证
文档复制为VIP权益,开通VIP直接复制
 信息提交成功
信息提交成功
