没有合适的资源?快使用搜索试试~ 我知道了~
2020-2021年中考化学分类汇编科学流程图1.doc
1.该资源内容由用户上传,如若侵权请联系客服进行举报
2.虚拟产品一经售出概不退款(资源遇到问题,请及时私信上传者)
2.虚拟产品一经售出概不退款(资源遇到问题,请及时私信上传者)
版权申诉
0 下载量 196 浏览量
2021-12-10
01:10:14
上传
评论
收藏 572KB DOC 举报
温馨提示

试读
17页
2020-2021年中考化学分类汇编科学流程图1.doc
资源推荐
资源详情
资源评论
2020-2021 年中考化学分类汇编科学流程图 1
一、化学科学流程图
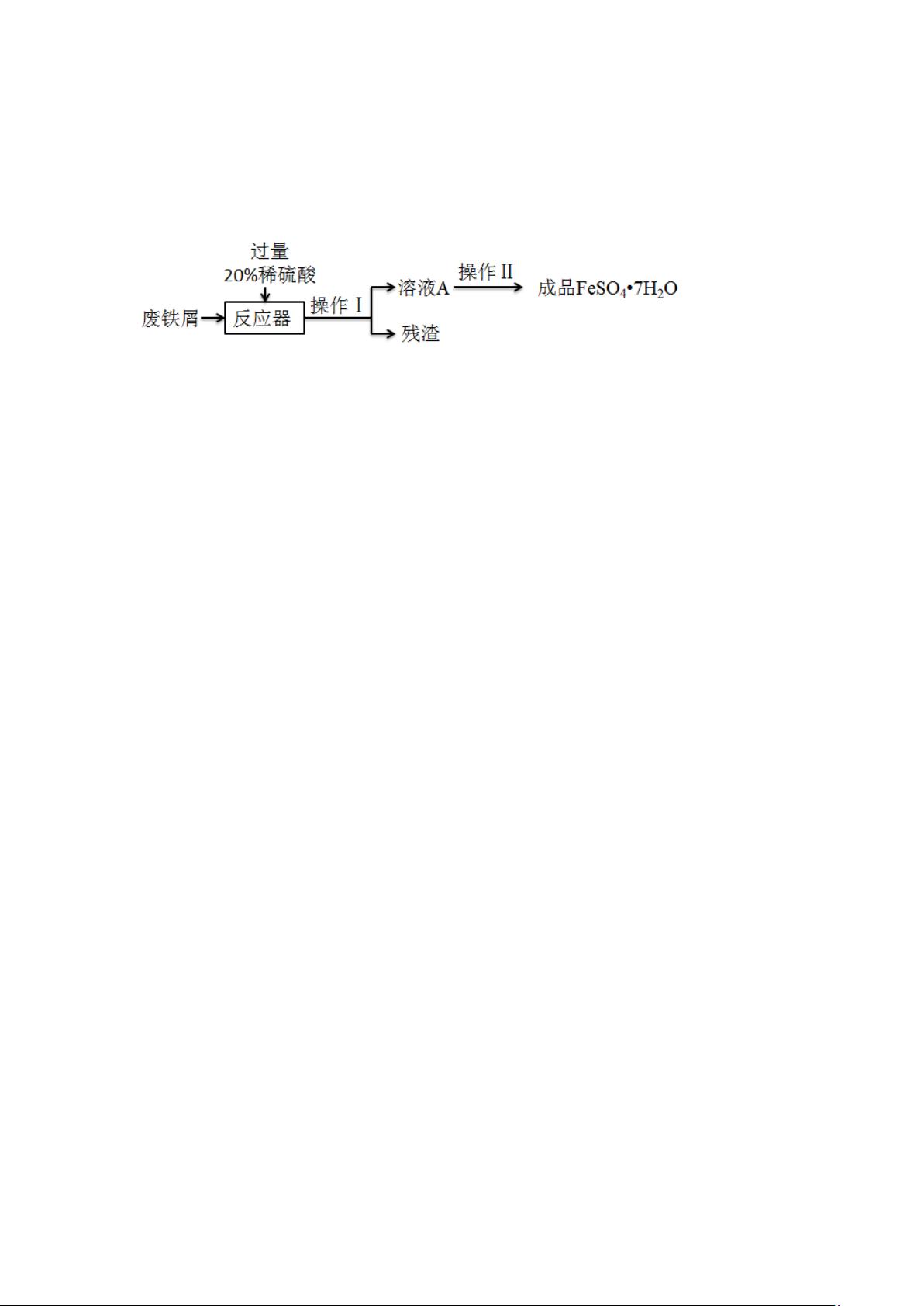
1.废铁屑的主要成分是铁,同时还有少量铁锈(主要成分是
Fe
2
O
3
)等杂质,动物饲料硫
酸亚铁的生产工艺之一如图所示:
(
1
)实验室欲用
98%
的浓硫酸(密度
1.84g/mL
)配制
200g20%
的稀硫酸,有以下实验步
骤:
a.
量取
b.
计算
c.
稀释
d.
装瓶贴标签
正确的顺序是
_____
(填字母)。若用量筒量取浓硫酸时俯视读数,其他操作正确,则所得
溶液的质量分数
_____20%
(填“>”“<”或“=”)。
(
2
)在反应器中反生的化学反应①
Fe
2
O
3
+
3H
2
SO
4
=
Fe
2
(SO
4
)
3
+
3H
2
O
;②
Fe
2
(SO
4
)
3
+
Fe
=
3FeSO
4
;③
_____
。
(
3
)溶液
A
中的溶质是
_____
(填化学式)。
(
4
)操作Ⅰ的名称是
_____
,完成操作Ⅰ的玻璃仪器有:玻璃棒、烧杯和
_____
。
(
5
)经过操作Ⅱ:蒸发浓缩、
_____
、过滤、冰水洗涤、低温干燥可得硫酸亚铁晶体
(
FeSO
4
•
7H
2
O
),用低温干燥说明硫酸亚铁晶体可能具有的性质是
_____
。
【答案】
bacd
<
Fe
+
H
2
SO
4
=
FeSO
4
+
H
2
↑
FeSO
4
、
H
2
SO
4
过滤
漏斗
降温结晶
受
热易分解(或受热不稳定或受热易发生化学变化等)
【解析】
【详解】
(
1
)实验室欲用
98%
的浓硫酸(密度为
1.84g/mL
)配制
200g20%
的稀硫酸,实验步骤:
计算、量取、稀释和装瓶贴标签。所以正确的顺序是
bacd
.若用量筒量取浓硫酸时俯视读
数,则量取的液体偏少,即溶质偏少,则所得溶液的质量分数<
20%
。
(
2
)在反应器得到的生成物最终得到硫酸亚铁,所以过程中氧化铁和硫酸反应生成硫酸铁
和水,而硫酸铁和铁反应生成硫酸亚铁,还可以有铁和硫酸反应生成硫酸亚铁和氢气,所
以发生的化学反应①
Fe
2
O
3
+3H
2
SO
4
=Fe
2
(
SO
4
)
3
+3H
2
O
;②
Fe
2
(
SO
4
)
3
+Fe=3FeSO
4
;
③
Fe+H
2
SO
4
=FeSO
4
+H
2
↑
(
3
)由于在反应器得到的生成物最终得到硫酸亚铁且加入的硫酸过量,所以溶液
A
中的
溶质是
H
2
SO
4
、
FeSO
4
。
(
4
)操作
I
实现了固体和液体分离,为过滤,完成操作
I
的玻璃仪器有:玻璃棒、烧杯和
漏斗。
(
5
)经过操作
Ⅱ
:蒸发浓缩
降温结晶、过滤、冰水洗涤、低温干燥可得硫酸亚铁晶体
(
FeSO
4
•7H
2
O
),用低温干燥说明硫酸亚铁晶体可能具有的性质是
热不稳定或者受热易分
解。
故答案为
(
1
)
bacd
;<。
(
2
)①
Fe
2
O
3
+3H
2
SO
4
=Fe
2
(
SO
4
)
3
+3H
2
O
;②
Fe
2
(
SO
4
)
3
+Fe=3FeSO
4
;或者
Fe+H
2
SO
4
=FeSO
4
+H
2
↑
;
(
3
)
H
2
SO
4
、
FeSO
4
。
(
4
)过滤;漏斗。
(
5
)降温结晶;热不稳定或者受热易分解。
2
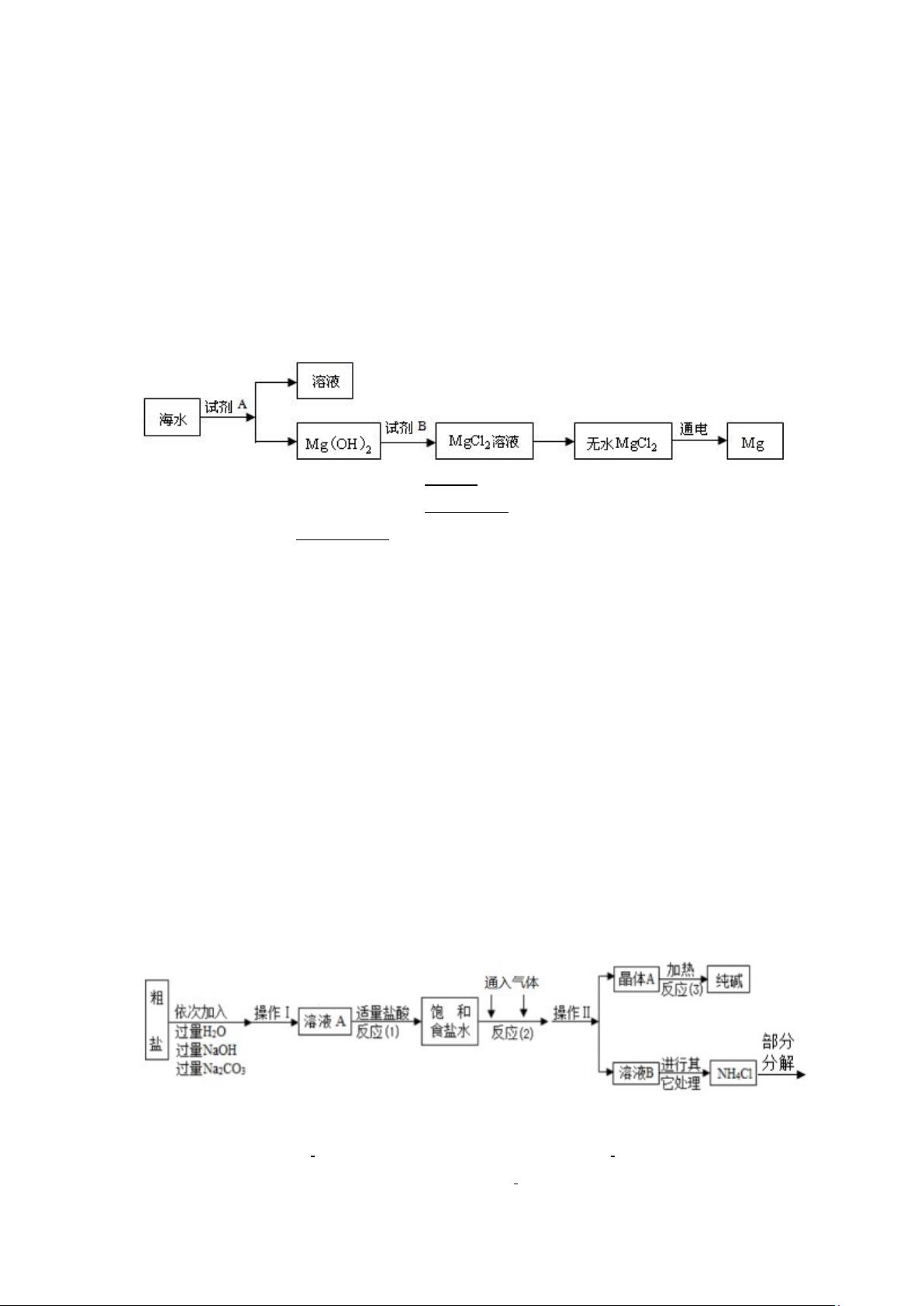
.海水是一种重要的自然资源(海水中含
NaCl
、
MgCl
2
等物质),被誉为
“
国防金属
”
的镁
主要是从海水中提取的,下面是从海水中提取金属镁的简单流程.
(
1
)从海水中获得淡水,常用的方法是
.
(
2
)从海水中获得粗盐,可将海水进行
.
(
3
)试剂
A
最好选用
.
【答案】(
1
)蒸馏.(
2
)蒸发结晶.(
3
)熟石灰.
【解析】
试题分析:(
1
)从海水中获得淡水,常用的方法是蒸馏.(
2
)从海水中获得粗盐,可将
海水进行蒸发结晶.(
3
)氢氧化钙显碱性,能和氯化镁反应生成氢氧化镁沉淀,氢氧化钙
的价格比较经济.故填:熟石灰.
考点:对海洋资源的合理开发与利用;蒸发与蒸馏操作.
3.碳酸钠在轻工、建材、纺织、国防、医药等工业中有重要的应用
,
我国化学家侯德榜创
立了著名的
“
侯氏制碱法
”
,促进了世界技术的发展。
(查阅资料)①生产原料粗盐中含有少量可溶性杂质
(MgCl
2
和
CaC1
2
)
及不溶性杂质。
②氨气极易溶于水,二氧化碳能溶于水。
③生产原理
:NaCl + NH
3
+ CO
2
+ H
2
O = NaHCO
3
↓+ NH
4
C1
,分离得晶体
A
,并使其充分受热,
可分解制得纯碱及两种常见的氧化物。
④氯化铵分解的化学方程式是
NH
4
Cl===NH
3
↑+HCl↑
。
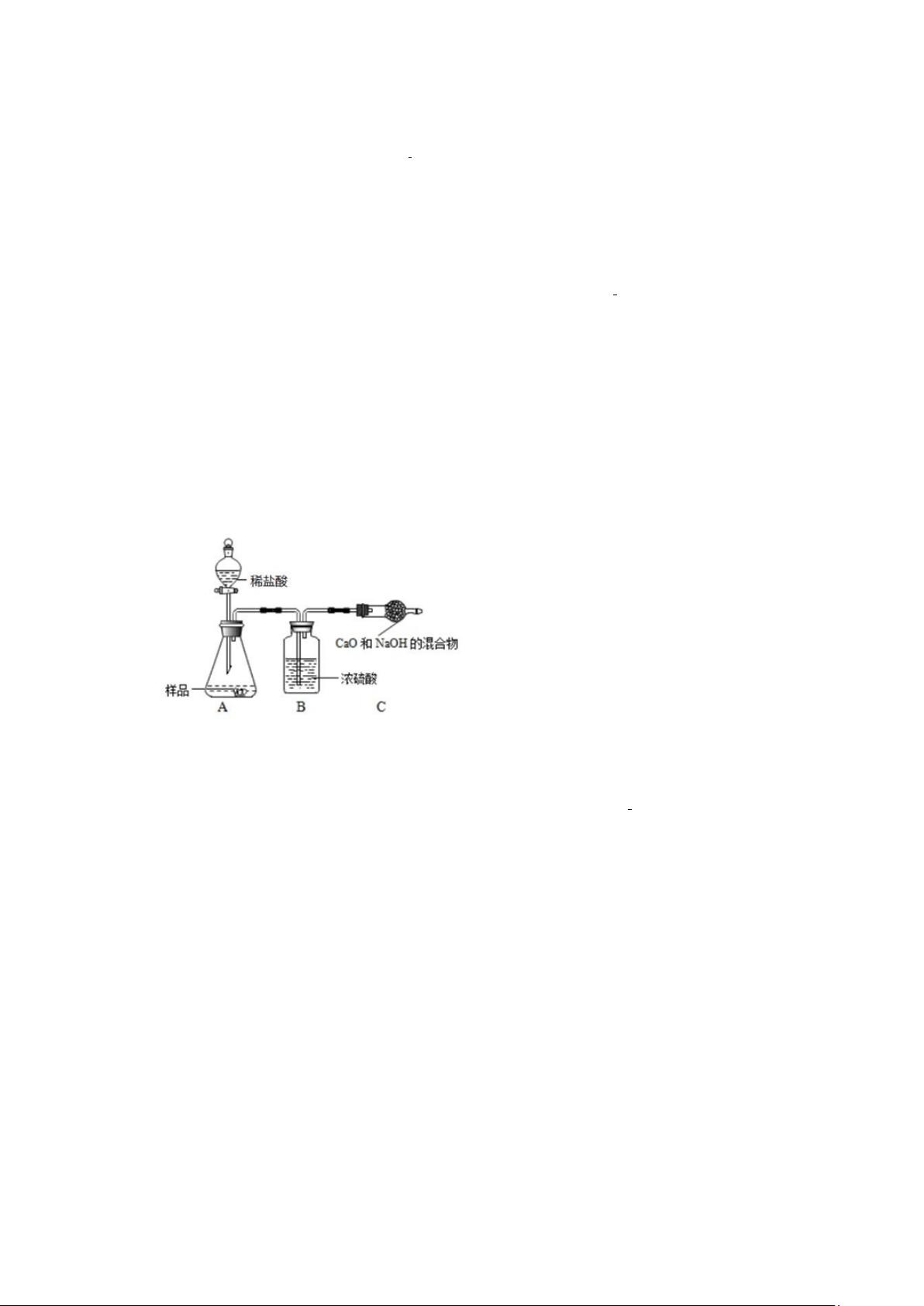
⑤部分生产流程如下图所示
:
(问
题讨论)
(
1
)溶液
A
中的溶质为
________
,流程中加入适量盐酸的作用是
________
。
(
2
)反应(
2
)中为提高产率,所通入气体的顺序是
________
(填字母序号).
A
.先通入
CO
2
再通入
NH
3
B
.先通入
NH
3
再通入
CO
2
(
3
)上述生产流程中可循环使用的是
________
(填序号).
A
.
CO
2
B
.
NH
3
C
.
HCl D
.
NaOH E
.
Na
2
CO
3
(组成确定)
(
1
)称取一定质量的纯碱样品,多次充分加热,称重,质量无变化;
(
2
)另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀
HNO
3
,再滴
加
AgNO
3
溶液,有白色沉淀。由上述实验可确定纯碱样品含有杂质
________
(写化学
式).
(含量测定)
同学们为了测定该纯碱样品的纯度(假定只含一种上述杂质),设计了如下
三组实验。甲组:取
12.0g
纯碱样品,向其中加入过量的盐酸,直至样品中无气泡冒出。
将反应所得溶液小心蒸发,并将所得物质干燥、冷却至室温称得固体质量为
13.1g
.样品中
碳酸钠的质量分数为
________
。
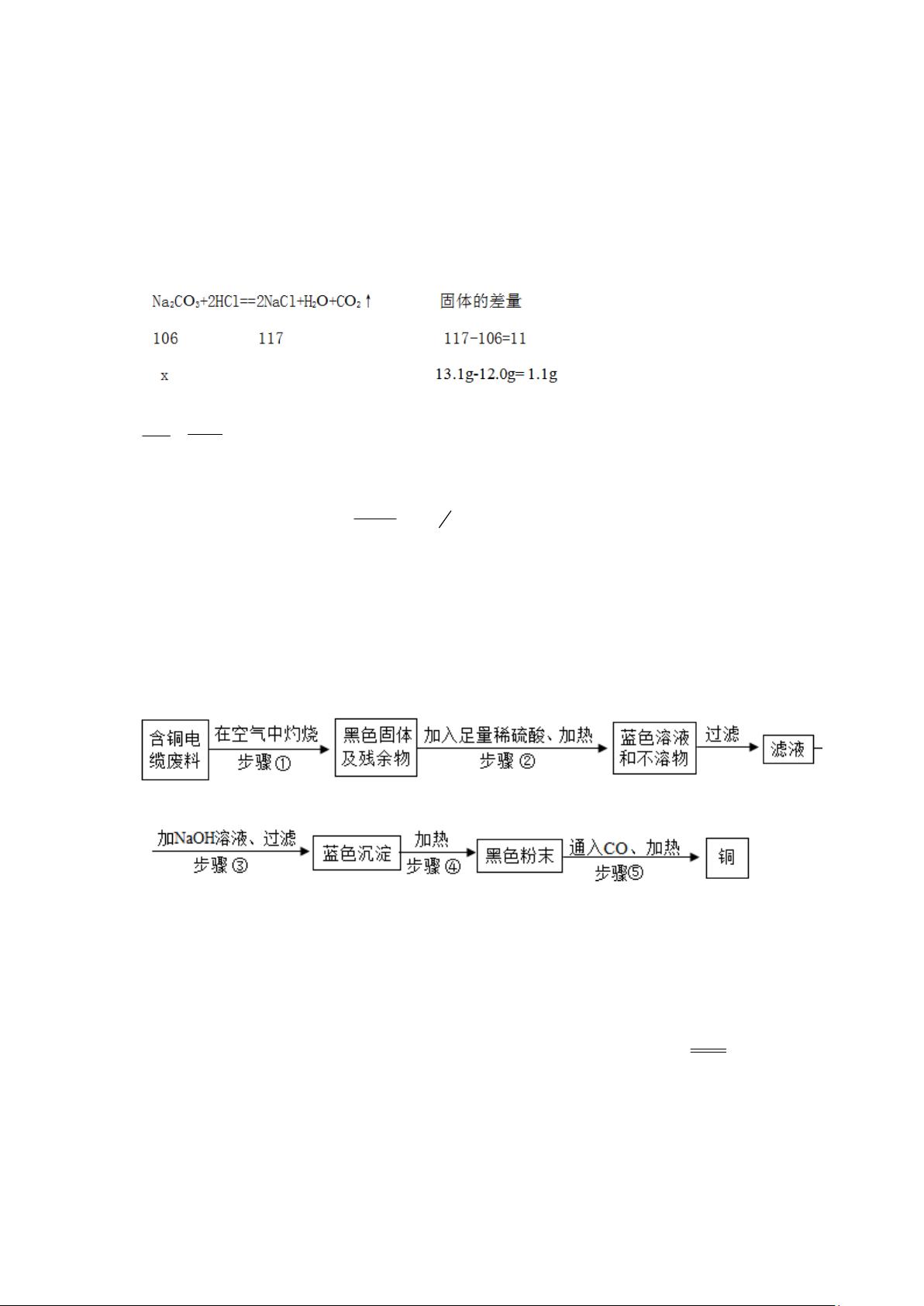
乙组:取
12.0g
纯碱样品,利用下图所示装置,测出反应装置
C
增重了
4.1g
(所加试剂均
足量
,
每一步都反应完全).实验结束,发现乙组测定的质量分数偏小,其原因是
_________
。
丙组:取
12.0g
的纯碱样品,完全溶于水,向其中加入过量的氯化钙溶液,待完全沉淀过
滤、
洗涤、烘干称量固体质量,从而计算出碳酸钠的质量分数。组内同学提出意见,认为
如果将氯化钙溶液换成氯化钡溶液则更好,老师认为有道理,原因是
________
。
【答案】
NaCl
、
NaOH
、
Na
2
CO
3
;
将氢氧化钠、碳酸钠转化成氯化钠;
B
;
ABCE
;
NaCl
;
88.3%
;
生成的二氧化碳气体没有被
C
中的烧碱完全吸收。
同质量的碳酸钠生
成碳酸钡的质量远大于碳酸钙,称量误差小。
【解析】
【分析】
【详解】
问题讨论:(
1
)粗盐中含有少量可溶性杂质(
MgCl
2
和
CaCl
2
),氯化镁能与氢氧化钠反应
生成氢氧化镁沉淀和氯化钠,氯化钙能与碳酸钠反应生成碳酸钙沉淀和氯化钠,所以
A
中
的溶质主要是氯化钠,由于氢氧化钠和碳酸钠过量,溶液
A
中也有氢氧化钠和碳酸钠;
过量的氢氧化钠、碳酸钠对于氯化钠来说仍是杂质,氢氧化钠和盐酸反应生成氯化钠和
水,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,所以流程中加入适量盐酸的作用是:
将氢氧化钠、碳酸钠转化成氯化钠;
(
2
)二氧化碳是酸性气体,在碱性溶液中的溶解度较大,所以先通入
NH
3
再通入
CO
2
,故
选
B
;
(
3
)根据生产流程中涉及的方程式和流程图,发现二氧化碳、氨气、氯化氢、碳酸钠为重
复使用的物质,故选
ABCE
;
[组成确定]氯化银是不溶于稀硝酸的白色沉淀,加入硝酸银溶液生成白色沉淀,不溶于稀
硝酸,沉淀是氯化银沉淀,说明原碳酸钠中含有氯化钠;
[含量测定]甲组:设样品中碳酸钠的质量为
x
106
11
=
1.1
x
g
解得
x=10.6g
样品中碳酸钠的质量分数为:
0
0
10.6g
×100
12.0g
=88.3
%;
乙组:乙组测定的质量分数偏小,其直接原因是
C
装置增重少,可能原因是生成的二氧化
碳气体没有被
C
中的烧碱完全吸收;
丙组:因为同质量的碳酸钠生成碳酸钡的质量远大于碳酸钙的质量,称量误差小于碳酸
钙,计算出碳酸钠的质量分数误差也就越小。
4.某同学设计的
“
从含铜电缆废料中提取铜
”
的实验方案如下:
(
1
)过滤用到的玻璃仪器有
_____
、
_____
、
_____
.
(
2
)写出步骤③和步骤⑤发生反应的化学方程式:
步骤③:
_____
;
步骤⑤:
_____
.
(
3
)此方案中可能造成空气污染的步骤有
_____
.
【答案】烧杯
漏斗
玻璃棒
CuSO
4
+2NaOH
═
Cu
(
OH
)
2
↓+Na
2
SO
4
CuO+CO
加热
Cu+CO
2
①⑤
【解析】
【详解】
剩余16页未读,继续阅读
资源评论

syzxwb
- 粉丝: 0
- 资源: 1万+
上传资源 快速赚钱
 我的内容管理
展开
我的内容管理
展开
 我的资源
快来上传第一个资源
我的资源
快来上传第一个资源
 我的收益 登录查看自己的收益
我的收益 登录查看自己的收益 我的积分
登录查看自己的积分
我的积分
登录查看自己的积分
 我的C币
登录后查看C币余额
我的C币
登录后查看C币余额
 我的收藏
我的收藏  我的下载
我的下载  下载帮助
下载帮助

 前往需求广场,查看用户热搜
前往需求广场,查看用户热搜安全验证
文档复制为VIP权益,开通VIP直接复制
 信息提交成功
信息提交成功
